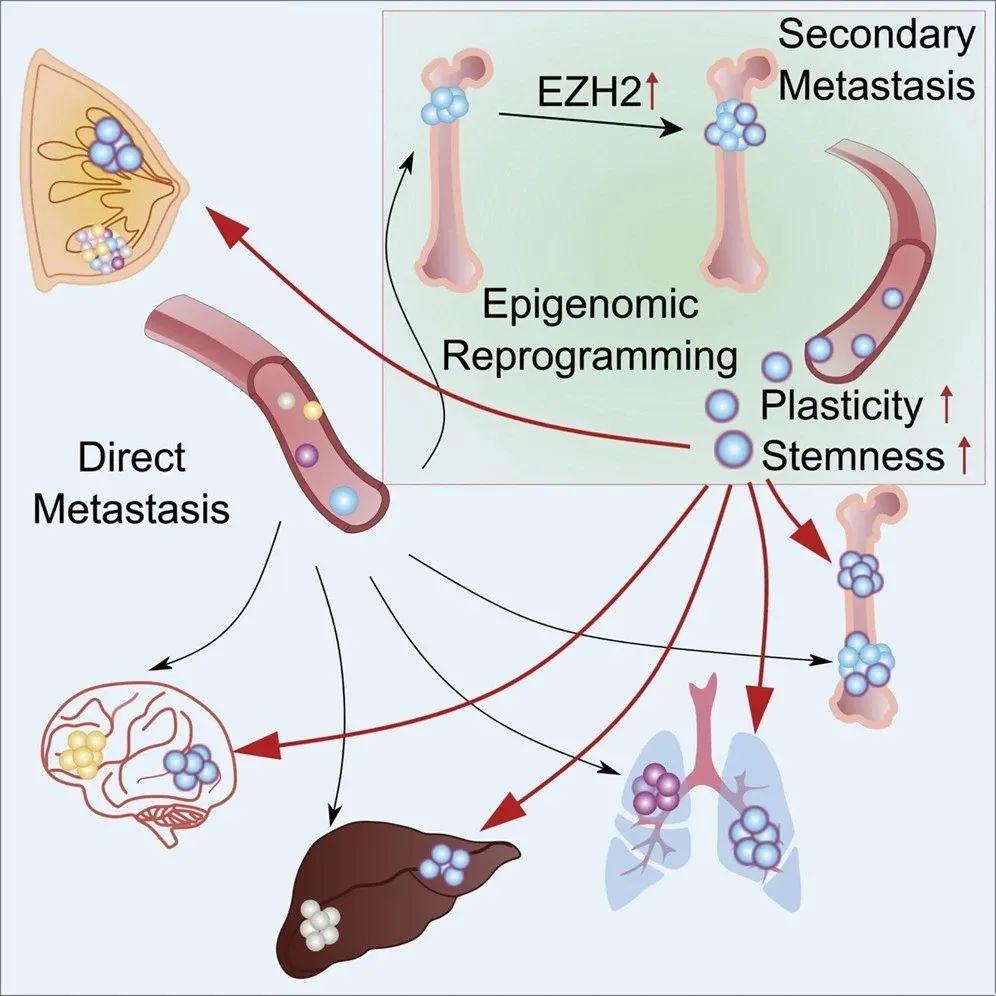
本文概要
困惑1:月经很久不来 就是绝经了吗?
乳腺癌术后辅助内分泌治疗的药物,是根据月经状态来决定的。成年女性月经状态大致分为绝经前,围绝经期,以及绝经后三种状态。一般来说,绝经前与围绝经期采用同一类治疗策略和药物,而绝经后则是另一类。我们不能单纯地认为月经不来就是绝经,中国很多女性常常因为子宫肌瘤而切除子宫,月经没了,但不代表绝经了。
绝经是一种卵巢衰竭且雌激素耗竭的状态,一般判断标准如下[1]:
(1)如果双侧卵巢已经切除(不管几岁),或60岁以上且1年以上没来月经,就可判定为绝经后。
(2)如果不到60岁且一年以上没来月经,还不足以判定绝经,得测雌二醇与FSH等水平来综合判断。
(3)如果不到45岁且没有切除卵巢,即便长期没来月经,也不应贸然判定为绝经。

困惑2:选择Tamoxifen/ target=_blank class=infotextkey>他莫昔芬,还是托瑞米芬?
他莫昔芬(三苯氧胺)是非常经典的内分泌药物,从1970年代使用至今。科学家试图通过改变他莫昔芬分子结构提高疗效,由此发明了托瑞米芬;但几乎所有试图证明托瑞米芬优于他莫昔芬的辅助临床试验都失败了[2,3]。因此,常规认为,他莫昔芬依然是金标准地位,托瑞米芬可能与其疗效相似,毒副反应各有不同。
他莫昔芬主要通过CYP2D6代谢酶代谢,而CYP2D6酶具有人群多样性和差异性,有的人酶活性低,有的人酶活性高,故科学家猜测CYP2D6基因多态性可能会引起他莫昔芬代谢物浓度差别[4]。为验证假设,在欧美乳腺癌前瞻性人群中开展验证性研究,结果大多数研究都发现CYP2D6酶代谢高低或CYP2D6基因检测结果并不影响他莫昔芬疗效[5-7];鉴于基因多态的种族特异性,还需在东亚人群中验证,相关临床试验(非低质量回顾性研究)发现,按照CYP2D6酶活力调整用药,依然不影响他莫昔芬疗效[8]。由此,用CYP2D6基因多态指导他莫昔芬用药的“假说”并未得到证明。
在临床实践中,我既不鼓励患者测定CYP2D6分型,也从来不用这个不成熟的指标去指导辅助内分泌用药;国际NCCN、国内CBCS等指南也均秉承这一观点[9-10]。
困惑3:是打卵巢功能抑制针,还是干脆卵巢切掉算了?
目前,对中高危绝经前激素受体阳性乳腺癌,医生会建议卵巢功能抑制。去除卵巢功能有两种途径:一是应用药物如促性腺激素释放激素类似物(LHRHa或GnRHa),使卵巢休眠;二是直接放疗破坏或手术切除卵巢,连根拔除。这两种方法是等效的,不存在谁好谁坏[11]。
但一般情况下,我更推荐卵巢功能抑制药物,毕竟停针后卵巢功能还能恢复。但在某些特定情况下,我也会考虑切除卵巢,如年龄46岁以上且非常高危,预计要打5-10年卵巢抑制针,等打完都50好几了,那时已自然绝经,就当下切掉算了,更方便也更经济。但对年轻女性不建议切卵巢。要知道,雌激素具有两面性,一方面是促进激素受体阳性乳腺癌细胞增殖的恶魔,另一方面也是维护骨质骨密度、保护心血管功能、调适良好心境的天使[12]。治疗乳腺癌时,我们要充分抑制雌激素;但治疗完成后,我们要恢复其生理角色。
困惑4:如何监测卵巢功能抑制针的疗效?
卵巢功能抑制针的监测和效果,我分享两点“猫论”:
第一,“薛定谔的猫”论,即抑制卵巢效果有不确定性。没有哪种卵巢功能针,能100%有效抑制。我碰到过进口LHRHa用药后,卵巢抑制依然不充分、雌激素很高的情况。不过这类情况发生率低,文献报道在5-10%[13,14]。故建议适时(注意不用很频繁,一般每6-12个月或者按照复查周期实施即可)检测雌激素全套,观察抑制充分与否。一旦抑制不佳,就得换药或切除卵巢。全程不检测、不监视雌激素抑制水平,对群体而言可能是无足轻重的,但对个人是意义重大的。
第二,“黑猫白猫”论,即只要有效果,就是好药。很多术后用药(包括化疗,靶向治疗,他莫昔芬,芳香化酶抑制剂)都无法直接确认疗效,到最后看复不复发才能判断有效无效,患者和医生都是“后知后觉”。但卵巢抑制针是个例外,它的作用是耗竭促性腺激素(FSH与LH),让雌激素枯竭,雌激素匮乏了,肿瘤细胞就“饿死”了,由此产生疗效[15]。所以,卵巢抑制针效果好不好,就看你使用后,月经还来不来,雌激素和FSH/LH水平低不低。如果对在用的卵巢抑制针不放心,就测个血,看看雌二醇和FSH水平是否很低,一目了然。
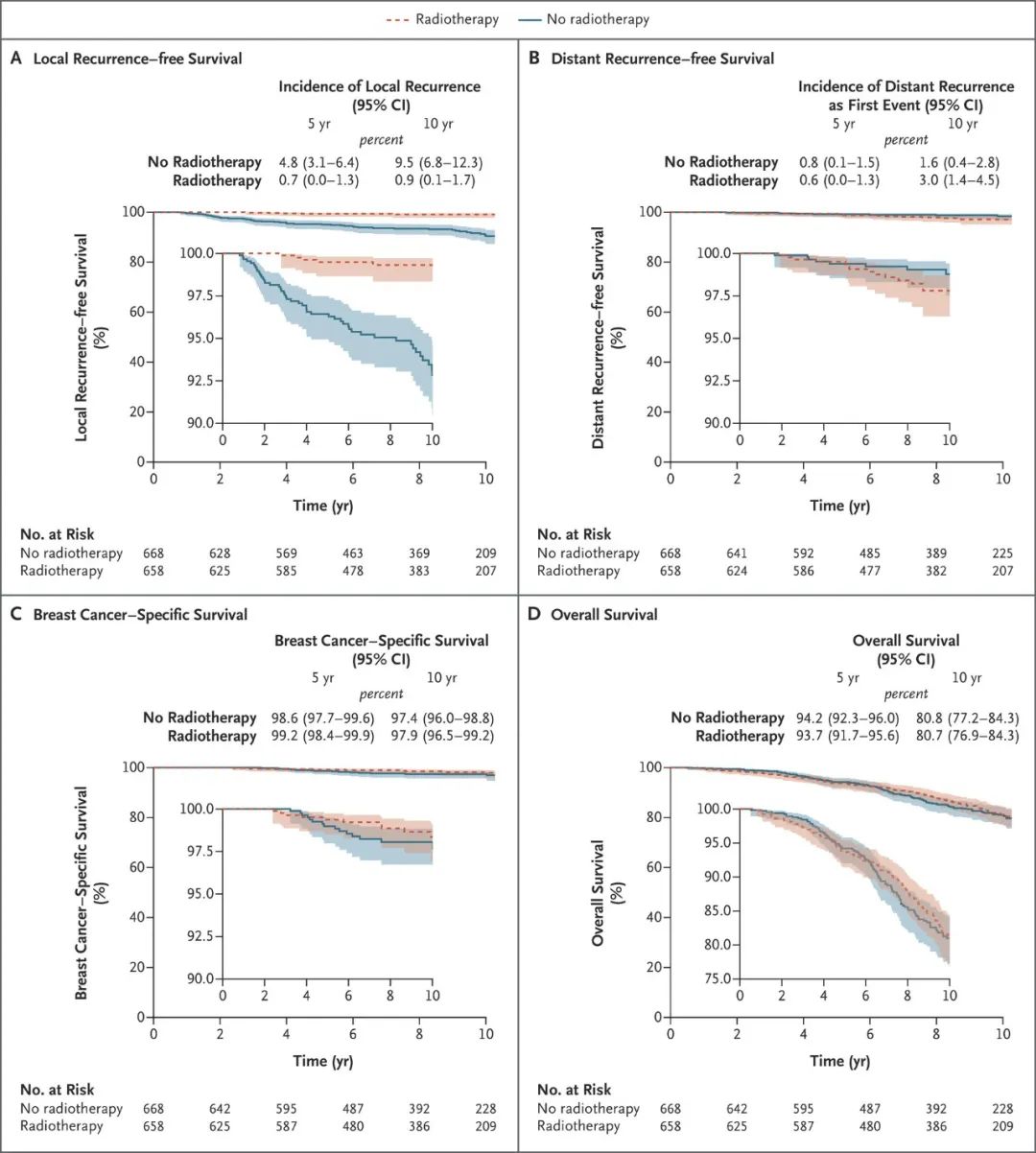
困惑5:内分泌治疗和放疗顺序怎么安排?
以非常严谨的角度,想证明内分泌和放疗的顺序,应通过临床试验。但因实施成本、研究者重视度、时间周期等因素,这方面的高级别证据并不多。我们来分别分析:
第一,绝经后,使用芳香化酶抑制剂(如阿那曲唑,来曲唑,依西美坦)的患者,前瞻性研究已证实,不管放疗同期还是放疗后用药,副反应没差别,疗效也差不多[16,17],所以可以大胆一起用。
第二,绝经前,使用他莫西芬的患者,虽然有回顾性研究提示两者能联用,对复发转移没影响,但放疗期间用他莫西芬可能会增加肺纤维化发生率[18]。因此为了降低毒性,就避开放疗。
第三,绝经前,使用卵巢功能抑制的患者,目前没有证据说不能联用,既可同期开始,也可以放疗后再卵巢抑制,没有大的关系[19]。
困惑6:术后哪些人需要用新药CDK4/6抑制剂?
CDK4/6抑制剂如阿贝西利、Palbociclib/ target=_blank class=infotextkey>哌柏西利,是“内分泌靶向治疗”范畴,随着相关药物进入医保,大家问得最多的是:我要不要使用CDK4/6抑制剂?这里提供4点用药参考:
(1)大多数患者尤其是淋巴结阴性患者,无需使用。
(2)高危激素受体阳性患者才可能用到,尤其是淋巴结转移4枚及以上的,推荐使用。
(3)淋巴结转移1-3枚的患者,需伴有其他高危因素如肿瘤大(5cm以上),组织学级别高(如III级),才考虑,同时也兼顾一下经济能力、年龄,以及对治疗的期待值[20,21]。
(4)有的患者一开始疾病很重,做了术前化疗,术后发现肿瘤或淋巴结转移还存在,也可酌情使用。
困惑7:选择哪一款CDK4/6抑制剂?
药物的选择,是非常讲证据的。选Palbociclib/ target=_blank class=infotextkey>哌柏西利还是阿贝西利,按照如下两个原则:
(1)术后患者,为了强化内分泌治疗,预防复发转移,这时候应该推荐阿贝西利。因为有临床试验证实阿贝西利是有效的[20],而哌柏西利尚待更多的数据[21]。
(2)晚期患者或术后复发转移患者,需长期维持内分泌治疗,既可以选择哌柏西利,也可以选择阿贝西利,因为有相关临床试验证实两个药都有效[22,23]。但两者的毒副反应各异,前者要重点管理血液学毒性,后者要重点防治消化道腹泻反应。
困惑8:内分泌治疗期间,能不能接种新冠疫苗、流感疫苗、HPV宫颈疫苗等?
内分泌治疗一段时间达到生理稳定状态后,理论上上述疫苗都可接种。白细胞特别是淋巴细胞数目是重要的判断指标,只有淋巴细胞充足,才能产生免疫效应,诱导出保护性抗体,不然打了疫苗没有效果,钱就打水漂了。我如下分类说明:
(1)卵巢功能抑制剂、他莫昔芬、芳香化酶抑制剂等药物,本身不会降低白细胞,这些药物治疗期间,可以妥妥接种[24]。但要和放化疗间隔一定时间(如6个月后)。
(2)CDK4/6抑制剂如阿贝西利、哌柏西利等有降低白细胞的毒副反应,此时淋巴细胞的量可能不足,接种疫苗要慎重。我临床看到使用阿贝西利后,白细胞大概会降低到3000左右(正常参考值>4000),如果低于2000,建议升白处理,此时也不应该接种疫苗;如果长期维持在3000以上,则可酌情考虑接种疫苗。CDK4/6抑制剂期间接种疫苗后,还是能诱导出保护性抗体的,虽然浓度略微低于正常女性[25]。
余科达 主任医师
教授 博士生导师
参考文献: